Solidificação é o processo físico em que uma amostra no estado líquido passa para o estado sólido. É um processo exotérmico e que depende de trocas de calor que façam a amostra ceder energia até atingir seu ponto de mudança. Nessa etapa, muitas substâncias sofrem também um processo de contração, devido à proximidade maior entre as moléculas. Toda amostra possui uma temperatura bem definida para se solidificar, chamada de ponto de solidificação. Na água, esse processo ocorre em 0 °C.
Leia também: Quais são as mudanças de estado físico da matéria?
Tópicos deste artigo
- 1 - Resumo sobre solidificação
- 2 - O que é solidificação?
- 3 - Como ocorre a solidificação?
- 4 - Características da solidificação
- 5 - Ponto de solidificação
- 6 - O que causa a solidificação?
- 7 - Mudanças de estado físico da água
- 8 - Exercícios sobre solidificação
Resumo sobre solidificação
- Solidificação é a transformação do estado líquido para o sólido.
- A solidificação depende da redução da energia térmica do corpo.
- É um processo exotérmico e pode causar a contração da substância.
- Todo corpo passa pela solidificação ao atingir uma temperatura específica.
- A solidificação ocorre na água em 0 °C.
O que é solidificação?
A solidificação é um processo físico-químico responsável pela mudança do estado físico líquido para o estado físico sólido. É o processo inverso da fusão, de natureza exotérmica, ou seja, a amostra precisa ceder energia térmica.
Existem diversos exemplos da aplicação prática da solidificação:
a) Formação de gelo: a água passa pelo processo de solidificação para formar o gelo, como pode ser observado em uma geleira, em um processo natural, ou em refrigeradores, em um processo artificial.

b) Rochas vulcânicas: a lava vulcânica, após sair do solo, sofre um intenso processo de resfriamento e forma com isso variadas espécies de rochas vulcânicas.

c) Siderurgia: a composição de ligas metálicas, formadas em indústrias siderúrgicas, ocorre com a junção de diversos tipos de metais fundidos para que, na solidificação, formem materiais mais resistentes e temperados.

Como ocorre a solidificação?
O processo de solidificação depende da redução de energia térmica do líquido. À medida que a energia cinética das moléculas diminui, ou seja, a temperatura, o movimento dessas moléculas fica mais lento e próximo entre si. Assim, a força de atração se intensifica e ocorre a formação da estrutura cristalina, por meio da energia de ligação intermoleculares.
![Estrutura cristalina de um sólido.[1]](https://s3.static.brasilescola.uol.com.br/be/2025/09/estrutura-cristalina-solido.jpg)
Características da solidificação
- Liberação de calor latente de solidificação: durante a mudança de estado, a temperatura da amostra permanece constante até que ela ceda todo o calor latente necessário para realizar a mudança de estado.
- Alteração do volume: a grande maioria das substâncias, no processo de solidificação, sofre processos de contração. A proximidade das moléculas na formação da rede cristalina pode diminuir o volume; porém, existem exemplos contrários, como a água, que aumenta ligeiramente seu volume na solidificação.
Leia também: Diferença entre calor sensível e calor latente
Ponto de solidificação
Para que ocorra a solidificação, é necessário que a amostra atinja uma temperatura específica, a depender de sua natureza e de um estado de pressão. É possível também que nessa temperatura objetos no estado sólido e líquido podem coexistir em equilíbrio térmico. Veja alguns exemplos para diferentes substâncias:
|
Substância |
Ponto de solidificação (0°C) Não pare agora... Tem mais depois da publicidade ;)
|
|
Água |
0 |
|
Ferro puro |
1538 |
|
Nitrogênio |
-210 Não pare agora... Tem mais depois da publicidade ;)
|
|
Etanol |
-114 |
|
Ouro |
1064 |
Uma forma prática de relacionar a temperatura de solidificação com diversos estados distintos de pressão é o diagrama de fases.

O que causa a solidificação?
A causa principal da solidificação é a remoção de calor, energia térmica, do sistema onde se encontra a amostra líquida. Essa perda de energia tem como consequência a diminuição da energia cinética de agitação das moléculas, tornando-as mais próximas. Com isso, a energia de ligação entre elas aumenta, formando a estrutura cristalina, e o líquido se transforma em sólido.
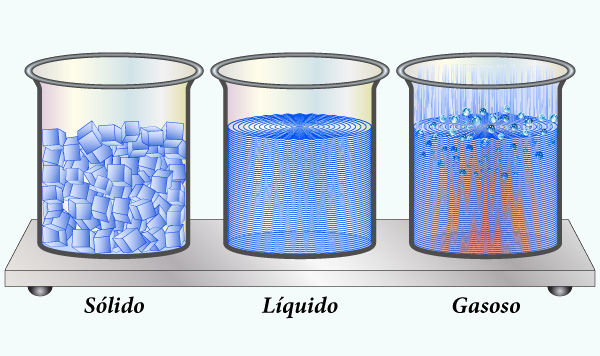
Mudanças de estado físico da água
No ciclo da água, a solidificação é conhecida como congelamento e ocorre quando o líquido perde calor suficiente para chegar em 0°C. Nesse ponto, a amostra líquida precisa ceder, em uma condição normal de pressão, uma quantidade específica de 80 calorias para cada grama. Na solidificação da água, de uma forma extraordinária, o gelo passa por um processo de dilatação e diminuição de sua densidade. Isso explica a formação de placas gelos na superfície de lagos e mares.
Exercícios sobre solidificação
1. (G1 - CPS 2014)
Uma atração turística da Áustria é Salzburgo, cidade natal de Mozart, construída na Antiguidade graças às minas de sal. Salzburgo significa castelo do sal, pois nessa cidade está localizada a mina de sal mais antiga do mundo, em atividade desde a Idade do Ferro (1000 a.C.).
No passado, o sal era um importante e quase insubstituível conservante alimentar e, além de cair bem ao nosso paladar, ele é uma necessidade vital, pois, sem o sódio presente no sal, o organismo seria incapaz de transmitir impulsos nervosos ou mover músculos, entre eles o coração.
(terra.com.br/turismo/roteiros/2000/11/10/009.htm Acesso em: 16.08.2013. Adaptado)
O sal também pode ser obtido da água do mar, processo que ocorre em salinas.

Durante a obtenção de sal em uma salina,
a) a água sofre evaporação.
b) a água sofre sublimação.
c) o sal sofre fusão.
d) a água e o sal sofrem sublimação.
e) a água e o sal sofrem solidificação.
Resposta:
Letra A. Nas salinas, a água do mar é represada. Exposta ao Sol, essa água evapora, restando o sal.
2. (PUC-RJ 2016) Uma quantidade de 750 mL de água a 90ºC é paulatinamente resfriada até chegar ao equilíbrio térmico com o reservatório que a contém, cedendo um total de 130 kcal para esse reservatório. Sobre a água ao fim do processo, é correto afirmar que:
Considere:
- calor específico da água líquida cágua = 1,0 cal/g ºC
- calor específico do gelo cgelo = 0,55 cal/g ºC
- calor latente de solidificação da água CL = 80 cal/g
- densidade da água líquida ρágua = 1,0 g/mL
a) a água se encontra inteiramente em forma de gelo.
b) a água se encontra a uma temperatura de 0 ºC.
c) a água se encontra inteiramente em estado líquido.
d) a temperatura final da água é de 4 ºC.
e) há uma mistura de gelo e água líquida.
Resposta:
[A].
\(Q = m \cdot c \cdot \Delta \theta\\ Q_1 = 750 \cdot 1 \cdot (90-0)\Rightarrow Q_1 = 65,5 \cdot 10^3 cal\Rightarrow Q_1 = 65,5 kcal\)
\(Q = m \cdot L\\ Q_2 = 750 \cdot 80\Rightarrow Q_2 = 60 \cdot 10^3 cal\Rightarrow Q_2 = 60 kcal\)
O enunciado diz que a água cedeu 130 kcal, que é maior que o gasto de Q1 + Q2 até solidificar totalmente. Portanto, a temperatura final da água é menor que 0 ºC, encontrando-se inteiramente em forma de gelo.
Créditos da imagem
Fontes
HALLIDAY, David; RESNICK, Robert; WALKER, Jearl (colab.). Fundamentos de física: gravitação, ondas e termodinâmica. Volume 2. 10. ed. Rio de Janeiro: LTC - Livros Técnicos e Científicos, 2016.
HEWITT, P. G. Física conceitual. 9. ed. Porto Alegre: Bookman, 2002.

