Elementos de transição são os metais situados entre os grupos 3 e 12 da Tabela Periódica, caracterizados quimicamente por possuírem os subníveis d ou f incompletos em sua configuração eletrônica. Eles são divididos em transição externa, que ocupam o bloco d, e transição interna, conhecidos como lantanídeos e actinídeos, que pertencem ao bloco f. Essa característica estrutural os diferencia dos elementos representativos e influencia diretamente suas propriedades químicas e físicas.
Leia também: Quais são as famílias da Tabela Periódica?
Tópicos deste artigo
- 1 - Resumo sobre elementos de transição
- 2 - O que são os elementos de transição?
- 3 - Elementos de transição interna
- 4 - Elementos de transição externa
- 5 - Características dos elementos de transição
- 6 - Diferenças entre elementos de transição e representativos
- 7 - Como saber se um elemento é de transição?
- 8 - Exercícios resolvidos sobre elementos de transição
Resumo sobre elementos de transição
- Os elementos de transição são aqueles localizados entre os grupos 3 e 12 da Tabela Periódica.
- São caracterizados por apresentaram os subníveis d ou f incompletos em sua configuração eletrônica.
- É possível dividir os elementos de transição em transição externa (bloco d) e em transição interna (bloco f, lantanídeos e actinídeos).
- Todos os elementos de transição são metálicos e, assim, observamos propriedades como condutividade térmica, elétrica, maleabilidade e elevados pontos de fusão, de modo geral.
- Entretanto, especificidades surgem, como é o caso dos actinídeos (todos radioativos) e os metais nobres, como ouro e platina, que possuem uma baixíssima reatividade química.
O que são os elementos de transição?
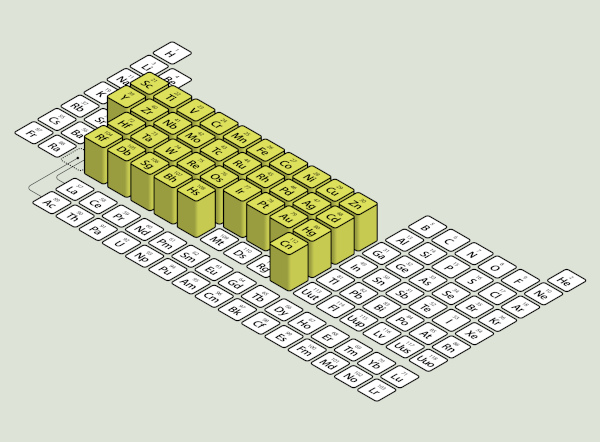
Elementos de transição são elementos que estão entre os elementos representativos da Tabela Periódica, ou seja, alocados nos grupos 3 ao 12. Como alguns autores defendem a ideia de que elementos de transição necessitam possuir subnível d incompleto, os elementos do grupo 12, para esses autores, não são considerados como elementos de transição.
Como todos os elementos de transição são metálicos, também é comum chamar tal grupo de elementos de metais de transição.
Os elementos de transição são divididos de duas formas: transição interna (elementos do bloco f) e transição externa (elementos do bloco d).
Elementos de transição interna
Os elementos de transição interna são os elementos do bloco f da Tabela Periódica, ou seja, os elementos contidos nos sexto e sétimo períodos do Grupo 3, também conhecido como lantanídeos e actinídeos.
A característica dos elementos de transição interna é, portanto, a presença do subnível f na distribuição eletrônica, sendo 4f para os lantanídeos e 5f para os actinídeos.

Elementos de transição externa
Os elementos de transição externa são os elementos do bloco d da Tabela Periódica, ou seja, todos os metais presentes nos grupos que vão de 3 a 12, excetuando-se, obviamente, os lantanídeos e actinídeos.
Alguns autores defendem que, para um elemento ser de transição externa, ele deve ter subnível d incompleto no estado fundamental, ou formar cátions estáveis com subnível d incompleto. Dessa forma, isso não colocaria os elementos do grupo 12 como elementos de transição, já que possuem configuração eletrônica final na forma ns2(n–1)d10 no estado fundamental (em que “n” representa o período que o elemento se encontra), e seus cátions estáveis, de carga +2, ainda apresentam o subnível d completo.

Características dos elementos de transição
Os elementos de transição possuem subnível d ou f incompletos em sua configuração eletrônica. Boa parte dos metais do bloco d forma espécies de carga +2 ou +3, enquanto os elementos do bloco f, na maioria das vezes, formam espécies de carga +3.
Todos os elementos de transição do sétimo período, incluindo os actinídeos, são radioativos, sendo que alguns deles sequer são encontrados na natureza e, por isso, são produzidos em laboratório, como é o caso de todos os elementos de transição de número atômico 104 a 112.
Pensando-se apenas nos elementos de transição externa, podemos dizer que quase todos os metais são duros, dúcteis, maleáveis, com grandes condutividades térmica e elétrica. São também menos voláteis que os metais representativos, com aumento pico de pontos de fusão para os elementos localizados no sexto período, entre os grupos 5 e 8. Lá estão os elementos de transição de maior ponto de fusão: tungstênio (3695 °C), rênio (3459 °C), ósmio (3306 °C) e tântalo (3290 °C).

Embora apresente algumas variações, percebe-se que a primeira energia de ionização para os elementos do bloco d é maior que para os metais do bloco s precedentes.
Quanto à reatividade, embora cada grupo possua suas especificidades, percebe-se que os elementos de transição externa são moderadamente reativos, formando compostos binários quando aquecidos com O2, enxofre ou halogênios. Ainda é possível a reação com H2, B, C ou N2 para a formação de hidretos, boretos, carbetos ou nitretos, respectivamente. Essa reatividade, entretanto, é mínima para alguns metais nobres, como prata, ouro, mercúrio e os metais do grupo da platina (Pt, Pd, Rh, Ir, Os e Ru). Em termos termodinâmicos, Ag, Au e Hg são os metais menos reativos conhecidos.
Os lantanídeos lembram bastante os elementos de transição externa. Possuem uma boa reatividade, reagindo lentamente com a água fria, porém rapidamente com ácidos. São bons agentes redutores, mas entram em ignição quando em contato com o ar.
Entre os lantanídeos, chama a atenção a contração lantânica, que é um decréscimo dos raios dos lantanídeos conforme ocorre o aumento do número atômico. Isso é consequência da atração nuclear ao subnível 4f.
Os actinídeos possuem uma química mais complicada, além do fato de apenas dois elementos apresentarem isótopos naturais: urânio e tório. Todos os actinídeos são tóxicos, como é o caso do 231Pa.
Diferenças entre elementos de transição e representativos
Existem duas formas de diferir elementos representativos de elementos de transição:
- Pela posição na Tabela Periódica
Elementos representativos são aqueles localizados nos grupos 1, 2 e de 13 até 18, enquanto os elementos de transição estão localizados entre os grupos 3 até 12.
- Pela configuração eletrônica
Os elementos representativos não possuem a presença de subníveis d ou f incompletos na sua configuração eletrônica. Os elementos dos grupos 1 e 2 terminam a configuração eletrônica em ns1 (grupo 1) ou ns2 (grupo 2), já os elementos que estão entre os grupos 13 até 18 terminam a configuração eletrônica na forma ns2npx, em que x pode ser 1, 2, 3, 4, 5 ou 6. Para ambos os casos, a letra “n” representa o período em que o elemento se encontra.
Como saber se um elemento é de transição?
Para saber se um elemento é de transição, deve-se observar se:
- ele se encontra entre os grupos 3 e 12 da Tabela Periódica;
- é um lantanídeo ou um actinídeo;
- se apresenta subnível d ou f incompleto na sua configuração eletrônica.
Caso um dos três critérios seja observado, pode-se afirmar que tal elemento é de transição.
Leia também: Quem são os metais alcalino-terrosos?
Exercícios resolvidos sobre elementos de transição
Questão 1
(UECE – 2ª Fase – 2º dia/2024.1) Considerando as propriedades dos elementos de transição, assinale a proposição verdadeira.
A) Os compostos dos elementos de transição são incolores devido às transições eletrônicas.
B) Todos os compostos de elementos de transição são diamagnéticos.
C) Apresentam apenas um estado de oxidação
D) Geralmente são dúcteis e maleáveis, bons condutores de calor e eletricidade.
Resposta: Letra D.
Sendo metálicos, os elementos de transição, de forma geral, apresentam características básicas dos metais, como ductilidade, maleabilidade, além de boa condução térmica e elétrica.
Questão 2
(UFGD/2015) Analisando-se as configurações eletrônicas a seguir, indique qual delas corresponde a um elemento de transição.
A) 1s22s22p63s1
B) 1s22s22p63s23p64s23d104p2
C) 1s22s22p63s23p64s23d8
D) 1s22s22p63s23p6
E) 1s22s22p63s23p64s2
Resposta: Letra C.
Elementos de transição possuem, na sua configuração eletrônica, subníveis d ou f incompletos, o que só se observa na espécie da alternativa C. Os demais são representativos.
Fontes
HOUSECROFT, C. E.; SHARPE, A. G. Inorganic Chemistry. 4. ed. Harlow (Inglaterra): Pearson Education Limited, 2012.
HAYNES, W. M. (ed.). CRC Handbook of Chemistry and Physics. 95a ed. CRC Press: 2014.
INTERNATION UNION OF PURE AND APPLIED CHEMISTRY. Nomenclature of Inorganic Chemistry: IUPAC Recommendations 2005. Edited by Neil G. Connelly et al. Cambridge: RSC Publishing, 2005. Disponível em: https://iupac.org/wp-content/uploads/2016/01/Red_Book_2005.pdf. Acesso em: 21 fev. 2026.


