Elementos radioativos possuem núcleos instáveis que emitem partículas alfa, beta e radiação para buscar equilíbrio, em um processo chamado decaimento radioativo. Tal processo ocorre naturalmente em elementos acima do número atômico 84 (polônio). Essas transformações seguem leis específicas, e cada isótopo possui um tempo de meia-vida próprio para sua desintegração.
São exemplos de elementos radioativos, de acordo com a IUPAC: rádio, plutônio, amerício, cúrio, berquélio, califórnio, einstênio, férmio, mendelévio, nobélio, frâncio e radônio. Elementos radioativos são fundamentais na medicina, em usinas nucleares e na indústria, mas exigem cautela rigorosa devido à sua natureza ionizante. Como podem danificar o DNA e causar doenças graves, seu uso é monitorado para que os benefícios tecnológicos superem os riscos biológicos e ambientais.
Leia também: Afinal, como funciona uma usina nuclear?
Tópicos deste artigo
- 1 - Resumo sobre elementos radioativos
- 2 - O que são elementos radioativos?
- 3 - Quais são os elementos radioativos?
- 4 - Classificação dos elementos radioativos
- 5 - Elementos radioativos na tabela periódica
- 6 - Características dos elementos radioativos
- 7 - Para que servem os elementos radioativos?
- 8 - Perigos dos elementos radioativos
Resumo sobre elementos radioativos
- Elementos radioativos são aqueles que possuem núcleos instáveis que emitem partículas e radiação (decaimento) para buscar estabilidade.
- São considerados como radioativos os elementos naturais a partir do polônio (Z=84) ou alguns isótopos sintéticos.
- Elementos radioativos se transformam em novos elementos ao emitir partículas alfa ou beta, conforme as leis de Soddy e Fajans.
- Têm aplicações vitais em diagnósticos médicos, tratamentos de câncer, geração de energia e datação de fósseis.
- Exigem manejo rigoroso, pois sua radiação ionizante pode causar mutações no DNA e danos graves à saúde.
O que são elementos radioativos?
Elementos radioativos são elementos que apresentam instabilidade nuclear, emitindo espontaneamente fragmentos do seu núcleo para adquirirem estabilidade. Nos elementos radioativos, as forças de repulsão exercidas pelos prótons superam as forças de intensas de atração que existem entre os prótons e os nêutrons (a chamada força forte), dessa forma, ocorre a emissão de partículas e radiação em um processo conhecido como decaimento radioativo.
Quais são os elementos radioativos?
Muito se fala que os elementos radioativos são os transurânicos, ou seja, aqueles com número atômico acima de 92, que é o número atômico do urânio. Contudo, sabe-se que, na verdade, todos os elementos a partir do polônio, Z = 84, são considerados radioativos. Porém, existem algumas exceções: o tecnécio, Tc, com número atômico 43 e o promécio, Pm, com número atômico 61.
A seguir, temos a lista dos elementos radioativos, de acordo com a Commission on Isotopic Abundances and Atomic Weights (CIAAW) da IUPAC.
|
Elementos radioativos Não pare agora... Tem mais depois da publicidade ;)
|
|||
|
Z |
Símbolo |
Elemento |
Número de massa dos isótopos radioativos |
|
43 |
Tc Não pare agora... Tem mais depois da publicidade ;)
|
tecnécio |
97, 98 |
|
61 |
Pm |
promécio |
145 Não pare agora... Tem mais depois da publicidade ;)
|
|
84 |
Po |
polônio |
209 |
|
85 |
At Não pare agora... Tem mais depois da publicidade ;)
|
astato |
210 |
|
86 |
Rn |
radônio |
222 Não pare agora... Tem mais depois da publicidade ;)
|
|
87 |
Fr |
frâncio |
223 |
|
88 |
Ra Não pare agora... Tem mais depois da publicidade ;)
|
rádio |
226 |
|
89 |
Ac |
actínio |
227 Não pare agora... Tem mais depois da publicidade ;)
|
|
92 |
U |
urânio |
234, 235 e 238 |
|
93 |
Np Não pare agora... Tem mais depois da publicidade ;)
|
netúnio |
237 |
|
94 |
Pu |
plutônio |
244 Não pare agora... Tem mais depois da publicidade ;)
|
|
95 |
Am |
amerício |
243 |
|
96 |
Cm Não pare agora... Tem mais depois da publicidade ;)
|
cúrio |
247 |
|
97 |
Bk |
berquélio |
247 Não pare agora... Tem mais depois da publicidade ;)
|
|
98 |
Cf |
califórnio |
251 |
|
99 |
Es Não pare agora... Tem mais depois da publicidade ;)
|
einstênio |
252 |
|
100 |
Fm |
férmio |
257 Não pare agora... Tem mais depois da publicidade ;)
|
|
101 |
Md |
mendelévio |
258 |
|
102 |
No Não pare agora... Tem mais depois da publicidade ;)
|
nobélio |
259 |
|
103 |
Lr |
laurêncio |
262, 266 Não pare agora... Tem mais depois da publicidade ;)
|
|
104 |
Rf |
rutherfórdio |
267 |
|
105 |
Db Não pare agora... Tem mais depois da publicidade ;)
|
dúbnio |
268 |
|
106 |
Sg |
seabórgio |
269, 271 Não pare agora... Tem mais depois da publicidade ;)
|
|
107 |
Bh |
bório |
270, 274 |
|
108 |
Hs Não pare agora... Tem mais depois da publicidade ;)
|
hássio |
269, 270 |
|
109 |
Mt |
meitnério |
277, 278 Não pare agora... Tem mais depois da publicidade ;)
|
|
110 |
Ds |
darmstádio |
281 |
|
111 |
Rg Não pare agora... Tem mais depois da publicidade ;)
|
roentgênio |
282 |
|
112 |
Cn |
copernício |
285 Não pare agora... Tem mais depois da publicidade ;)
|
|
113 |
Nh |
nihônio |
285, 286 |
|
114 |
Fl Não pare agora... Tem mais depois da publicidade ;)
|
fleróvio |
289, 290 |
|
115 |
Mc |
moscóvio |
288, 289, 290 Não pare agora... Tem mais depois da publicidade ;)
|
|
116 |
Lv |
livermório |
291, 292, 293 |
|
117 |
Ts Não pare agora... Tem mais depois da publicidade ;)
|
tennesso |
294 |
|
118 |
Og |
oganésson |
294 Não pare agora... Tem mais depois da publicidade ;)
|
Vale lembrar que quase todos os elementos da tabela periódica apresentam isótopos radioativos, o que quer dizer tais elementos apresentam espécies atômicas instáveis, embora o elemento em si não seja considerado radioativo.
Veja também: Acidente com césio-137 em Goiânia — maior acidente radiológico do mundo
Classificação dos elementos radioativos
Basicamente os elementos radioativos podem ser classificados em naturais ou sintéticos. Os elementos radioativos naturais são aqueles encontrados em fontes naturais, como o ar, água ou crosta terrestre. É o caso, por exemplo, do urânio, cuja principal fonte mineral é a pechblenda (uraninita).

Já os elementos radioativos sintéticos são aqueles produzidos por meio de reações nucleares, como reações de fusão nuclear ou bombardeamento de nêutrons, em laboratório. Essa é uma técnica muito comum para síntese de novos elementos, como os recentemente descobertos fleróvio (Fl), livermório (Lv), tenesso (Ts), moscóvio (Mc), nihônio (Nh) e oganessônio (Og). Este último, de número atômico 118, foi obtido por meio de uma reação de fusão nuclear na qual o isótopo cálcio-48 (Z = 20) foi bombardeado contra um alvo de califórnio-249 (Z = 98), que também produziu três nêutrons por núcleo de oganessônio produzido:
48Ca + 249Cf → 294Og + 3 1n
Elementos radioativos na tabela periódica
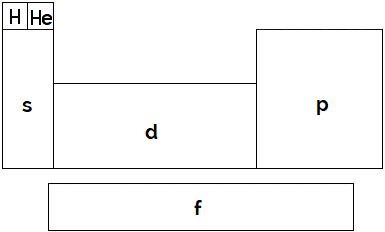
Na tabela periódica, identificam-se os elementos radioativos a partir do polônio, Z = 84. Contudo, não existe um grupo ou período específico para elementos radioativos, embora eles se concentrem entre os elementos mais pesados. A radioatividade também não é uma propriedade periódica. Vale salientar, entretanto, que algumas séries são totalmente radioativas, como é o caso dos actinídeos (que vão do número atômico 89 ao 103 na tabela periódica).

Algumas tabelas periódicas podem sinalizar que determinado elemento químico é radioativo, mas com o intuito de dizer que não existem isótopos estáveis (não radioativos) para aquele elemento.
Características dos elementos radioativos
Todo elemento radioativo é considerado instável e, dessa forma, naturalmente, eles ejetam fragmentos do seu núcleo e também emitem radiações para que possam adquirir maior estabilidade. Essa propriedade é conhecida como decaimento radioativo, a qual pode ser explica pelas leis da radioatividade, ou leis de Soddy e Fajans.
A primeira lei versa sobre o decaimento alfa, ou seja, quando um elemento radioativo emite uma partícula alfa, ele se transforma (fenômeno conhecido como transmutação) em um novo átomo, o qual possuirá duas unidades a menos de número atômico e quatro unidades a menos de número de massa. Isso decorre do fato da partícula alfa ser composta justamente por dois prótons e dois nêutrons (Z = 2 e A = 4), o que a faz, inclusive, ser representada, por vezes, como um núcleo de hélio (He).
\({}^{226}_{88}\mathrm{Ra} \;\rightarrow\; {}^{222}_{86}\mathrm{Rn} \;+\; {}^{4}_{2}\alpha\)
Já a segunda lei de Soddy e Fajans fala sobre o decaimento beta, ou seja, quando um elemento radioativo emite uma partícula beta, ele se transforma em um novo átomo, o qual manterá seu número de massa, mas terá uma unidade a mais de número atômico. Isso decorre do fato da partícula beta ser negativa e de massa desprezível, como um elétron (Z = -1 e A = 0).
\({}^{238}_{92}\mathrm{U} \;\rightarrow\; {}^{234}_{93}\mathrm{Np} \;+\; {}^{0}_{-1}\beta\)
Sabe-se que elétrons não estão no núcleo, contudo, entende-se que a partícula beta é consequência da desintegração de um nêutron, o qual produz uma partícula beta, um neutrino e um próton. O próton não é ejetado do núcleo, explicando, assim, o aumento do número atômico em uma unidade.

Outro ponto interessante acerca dos elementos radioativos é que tais elementos apresentam um tempo específico para decaimento, conhecido como tempo de meia-vida. O tempo de meia-vida é o tempo necessário para que a quantidade de um elemento radioativo caia pela metade. Esse valor é constante para cada elemento radioativo, sendo de grande interesse para avaliações cinéticas acerca do processo de desintegração.
Um exemplo é a utilização do tempo de meia-vida para saber o tempo necessário para que uma amostra radioativa decaia de tal forma que a quantidade remanescente seja insipiente, de modo que não ofereça mais riscos para os seres vivos e o meio ambiente.
Para que servem os elementos radioativos?
Diversos são os usos dos elementos radioativos. Inicialmente, é comum se pensar no seu uso para o campo de medicina, como no caso de exames de diagnóstico de imagem (como a tomografia e a radiografia), tratamentos clínicos (como a radioterapia), ou para geração de energia elétrica nas usinas nucleares. Contudo, os elementos radioativos também são muito úteis para a indústria e para áreas como agricultura, arqueologia, exploração espacial, geologia, entre outros.
-
Aplicações industriais dos elementos radioativos
Os usos de elementos radioativos na indústria são vastos. Uma técnica muito importante é a esterilização por irradiação, na qual alimentos, equipamentos médicos e outros materiais são expostos à radiação para desinfecção, sem causar qualquer dano no material irradiado e sem torná-lo radioativo. Técnicas de irradiação diminuem a utilização de substâncias químicas tóxicas nos processos de desinfecção.
Na agricultura, a utilização da radiação está intimamente ligada à melhora da produção de alimentos. Sementes são expostas à radiação para aprimoramento da espécie das plantas, as quais possuem mais resistência às populações de pragas e, assim, minimizando a utilização de pesticidas.
A radiação também pode ser utilizada como ferramenta medidora para determinar, por exemplo, a espessura de cascas de ovos, o que permite a separação daqueles que possuem cascas muito finas e mais propensas à ruptura antes de serem embalados. Filmes plásticos de polietileno, muito usados para revestimento de alimentos, também costumam ser irradiados para que possam suportar aquecimento acima do seu ponto de fusão usual.
O processo de medição com radiação também é comum para determinação da espessura de produtos de papel, níveis de fluidos em óleo e tanques de produtos químicos, além dos níveis de umidade e a densidade dos solos. Os raios x podem ser aplicados para detecção de defeitos imperceptíveis em soldas metálicas e para avaliação do escoamento de fluidos em motores selados. Essa capacidade de rastreamento de fluxo dos elementos radioativos também pode ser aplicada para detecção de vazamentos.
-
Aplicações médicas dos elementos radioativos
Os elementos radioativos são aplicados em diversos procedimentos para diagnóstico, monitoramento e tratamento de condições relacionadas à saúde humana. Há grande destaque para diagnóstico por imagem, como a radiografia ou a tomografia, exames imprescindíveis para determinação de protocolo de tratamento de um paciente. Esses equipamentos podem trazer boas imagens dos ossos, além de formas e detalhes de órgãos internos, ajudando médicos a localizarem e identificarem tumores ou outros problemas.

A radioterapia consiste na utilização de elementos radioativos para tratamento do câncer, buscando eliminar tecidos cancerosos, reduzir o tamanho de tumores ou os desconfortos físicos. O iodo radioativo, iodo-131, é muito utilizado para o tratamento do câncer de tireoide.
-
Usos acadêmicos e científicos dos elementos radioativos
É comum a utilização de elementos radioativos para servirem de marcadores em processos químicos, permitindo que os pesquisadores consigam visualizar o caminho tomado pelas substâncias, para a descrição mais precisa de uma rota reacional.
A inserção de marcadores radioativos em animais, plantas ou outros pontos de interesse do nosso planeta permite a visualização do comportamento das substâncias químicas em diversos ambientes, ajudando-nos em pesquisas relacionadas à agricultura, descoberta de poços de petróleo e descrição de correntes oceânicas, por exemplo.
Os arqueólogos fazem uso dos elementos radioativos para datação, permitindo estimar a idade de fósseis e outros objetos, com técnicas como a datação por carbono-14. A datação do solo também pode ser feita por elementos radioativos, auxiliando no estudo da geologia.
-
Uso de elementos radioativos em usinas nucleares

Alguns países se aproveitam da energia liberada na fissão de elementos radioativos para produção de energia elétrica. Nas usinas nucleares, a energia liberada no processo de fissão nuclear é utilizada para ebulir uma massa de água, de modo que o vapor produzido é aplicado em um gerador elétrico. O principal elemento usado como combustível nuclear é o urânio, o qual é colocado em pastilhas ou é selado em varas metálicas.
Saiba mais: Qual a diferença entre contaminação radioativa e irradiação?
Perigos dos elementos radioativos
Elementos radioativos produzem radiação ionizante que tem energia suficiente para afetar os átomos presentes nas células e, assim, danificar o material genético (DNA). Embora nossas células sejam muito capazes em reparar o dano, se este não for reparado de maneira correta, a célula pode vir a morrer ou se tornar cancerígena.

Exposição a altos níveis de radiação, como estar próximo a uma explosão atômica ou vazamento de fontes altamente radioativas, pode causar danos agudos à saúde, como queima da pele e síndrome da radiação aguda, que é caracterizada por náuseas e vômitos por horas, podendo resultar em óbito poucos dias ou semanas depois.
O nível de radiação elevado é, aproximadamente, o mesmo adquirido por se realizar 18 mil exames de raio X do tórax em todo seu corpo em algumas horas. Também podem ocasionar problemas de saúde em longo prazo, como câncer e doenças cardiovasculares. Exposição a níveis menores de radiação, como os encontrados na natureza, não causam danos imediatos à saúde, porém pode contribuir, mesmo que minoritariamente, para o risco de câncer.
Fontes
ATWOOD, D. Noble Gases: Inorganic Chemistry. In: Encyclopedia of Inorganic Chemistry. 2. ed. Wiley: Nova Jersey, 2005.
HAYNES, W. M. (ed.) CRC Handbook of Chemistry and Physics. 95a ed. CRC Press: 2014.
HOUSECROFT, C. E.; SHARPE, A. G. Inorganic Chemistry. 4. ed. Harlow (Inglaterra): Pearson Education Limited, 2012.
MIESSLER, G. L.; FISCHER, P. J.; TARR, D. A. Química Inorgânica. 5. ed. São Paulo: Pearson Education do Brasil, 2014.