As cadeias carbônicas são consequência da propriedade dos átomos de carbono de estabelecerem ligações covalentes entre si, dando origem a tais estruturas moleculares. Diversos são os arranjos tridimensionais que as cadeias carbônicas podem tomar, criando a demanda de classificar tais conformações estruturais para melhor compreensão e para melhor diferenciação. Por isso, aspectos estruturais básicos são utilizados para classificar as diversas cadeias carbônicas.
As cadeias carbônicas apresentam, em essência, quatro divisões: podem ser normais ou ramificadas, abertas ou fechadas, saturadas ou insaturadas, homogêneas ou heterogêneas. Tais classificações não são excludentes, mas, sim, cumulativas. De forma complementar, é comum também se debater a diferenciação entre sistemas aromáticos ou alifáticos para a classificação de cadeias carbônicas.
Leia também: Carbono — detalhes sobre um dos elementos químicos mais abundantes do Universo
Tópicos deste artigo
- 1 - Resumo sobre cadeias carbônicas
- 2 - O que são cadeias carbônicas?
- 3 - Classificação das cadeias carbônicas
-
4 - Classificação do carbono na cadeia
- → Classificação do carbono na cadeia quanto ao número de carbonos que um átomo de carbono se liga
- → Classificação do carbono na cadeia quanto à saturação/tipo de ligação
- → Classificação do carbono na cadeia quanto à geometria
- → Classificação do carbono na cadeia quanto à hibridização
- → Classificação do carbono na cadeia quanto à simetria (quiralidade)
- 5 - Exercícios resolvidos sobre cadeias carbônicas
Resumo sobre cadeias carbônicas
- Cadeias carbônicas são formadas a partir da capacidade do átomo de carbono de se ligar com outros átomos de carbono, criando estruturas moleculares diversas.
- Não há limite de tamanho para cadeias carbônicas, e, além disso, diversos são os arranjos tridimensionais que elas podem tomar, o que demandou um sistema específico de classificação.
- Para tais sistemas de classificação, são utilizados aspectos estruturais básicos das cadeias carbônicas.
- Cada cadeia pode carregar consigo até quatro classificações básicas.
- É comum, também, a diferenciação das cadeias entre alifáticas e aromáticas.
O que são cadeias carbônicas?

As cadeias carbônicas são consequência da propriedade dos átomos de carbono de estabelecerem ligações covalentes entre si, dando origem a tais estruturas moleculares. Essa propriedade é conhecida como catenação, e, apesar de não ser exclusiva do carbono, ele é o único que consegue criar cadeias diversas, sem limitação de tamanho e com grande estabilidade.
Classificação das cadeias carbônicas
Sem limitação de tamanho, as cadeias carbônicas são variadas e, para melhor compreensão, são classificadas de algumas formas básicas. Tais classificações não são excludentes, e, dessa forma, uma mesma cadeia pode acumular tais classificações.
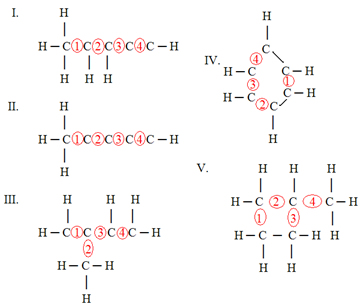
→ Cadeia normal ou cadeia ramificada
Entende-se que uma cadeia é normal quando, a partir de uma extremidade da cadeia carbônica, toma-se uma única direção até a outra extremidade. Por isso, é comum que as cadeias normais também sejam chamadas de lineares. Dentro das cadeias normais, são notados apenas carbonos primários ou secundários.
Entretanto, se algum dos carbonos internos da cadeia, ou seja, que não estão na extremidade, liga-se a um radical, a cadeia se torna ramificada. Ao se ligar com um radical, o carbono se torna terciário, enquanto, ao se ligar com dois radicais, o carbono se torna quaternário. Por isso, uma diferença das cadeias ramificadas em relação às cadeias primárias se dá na presença de carbonos terciários ou quaternários.

→ Cadeia aberta ou fechada
As extremidades de uma cadeia carbônica também são feitas por átomos de carbono. Se os átomos de carbono das extremidades não se ligarem, essa cadeia será considerada aberta. Entretanto, caso haja a ligação entre as extremidades da cadeia carbônica, com consequente formação de ciclos (ou de anéis), a cadeia é considerada como fechada. De modo simples, portanto, podemos dizer que não existem carbonos de extremidade em cadeias fechadas.

→ Cadeia saturada ou insaturada
As cadeias saturadas são aquelas em que os átomos de carbono apenas realizam, entre si, ligações covalentes simples. Do contrário, caso haja a presença de ligações duplas e/ou triplas entre átomos de carbono, classificamos a cadeia como sendo insaturada.

→ Cadeia homogênea ou heterogênea
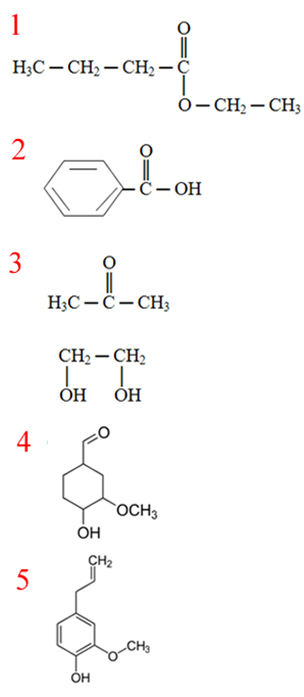
Quando pensamos em “homogêneo”, pensamos em continuidade. Dessa forma, cadeias carbônicas homogêneas são aquelas em que percebemos apenas átomos de carbono ao longo de toda a cadeia. Contudo, alguns átomos que necessitam de pelo menos duas ligações covalentes para se estabilizar podem substituir um átomo de carbono de dentro da cadeia, aparecendo entre, pelo menos, dois átomos de carbono.
Átomos que “substituem” átomos de carbono na cadeia são heteroátomos, justamente por proverem uma heterogeneidade à cadeia carbônica, quebrando, assim, a homogeneidade desta.

→ Cadeia aromática ou alifática
Existe uma modalidade de cadeia fechada específica que é conhecida como aromática. Analisadas estaticamente, as cadeias aromáticas apresentam ligações pi conjugadas, ou seja, alternadas. Porém, tais elétrons pi não se mantêm localizados em pontos específicos da cadeia aromática, mas, sim, deslocalizados, a fim de minimizar a repulsão eletrônica entre si e, assim, de trazer mais estabilidade para o composto.
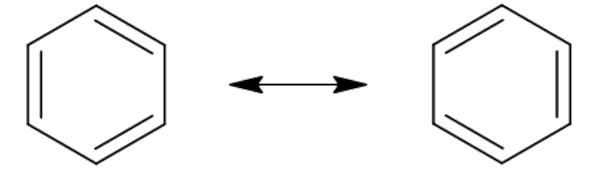
Uma cadeia, para ser aromática, além de fechada, deve apresentar todos os carbonos com hibridização sp2 (o que torna o composto planar), além de apresentar, quando analisada estaticamente, um número ímpar de ligações pi.

Todo e qualquer composto que não seja aromático é considerado como alifático. Alguns autores também utilizam a classificação alicíclico, para indicar compostos cíclicos (ou seja, de cadeia fechada) que são alifáticos.
Acesse também: Classificação das cadeias carbônicas — mais detalhes sobre essa classificação
Classificação do carbono na cadeia
Não só as cadeias carbônicas possuem classificação. Os carbonos dentro da cadeia também possuem classificações específicas.
→ Classificação do carbono na cadeia quanto ao número de carbonos que um átomo de carbono se liga

Os carbonos necessitam realizar quatro ligações covalentes para adquirirem estabilidade, segundo a regra do octeto. Dessa forma, um único átomo de carbono pode se ligar, simultaneamente, a até quatro átomos de carbono. Assim, define-se:
- Carbono primário: é o carbono que se liga até um átomo de carbono na cadeia carbônica. Ou seja, se um carbono na cadeia se liga a um único átomo de carbono, ou a nenhum, ele é classificado como primário. Alguns autores gostam de utilizar o termo “nulário” para o carbono que não se liga a nenhum átomo de carbono, trazendo uma pequena distinção para o carbono primário.
- Carbono secundário: é o carbono que se liga a dois átomos de carbono na cadeia carbônica.
- Carbono terciário: é o carbono que se liga a três átomos de carbono na cadeia carbônica.
- Carbono quaternário: é o carbono que se liga a quatro átomos de carbono na cadeia carbônica.
→ Classificação do carbono na cadeia quanto à saturação/tipo de ligação
Para alcançar as quatro ligações covalentes necessárias para adquirir estabilidade, os carbonos podem realizar ligações covalentes simples, duplas ou triplas.
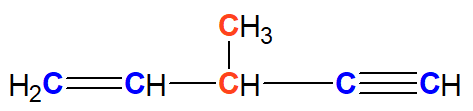
O carbono que só realiza ligações simples é chamado de carbono saturado. Já o carbono que apresenta alguma ligação pi, ou seja, a presença de ligações duplas ou triplas, é chamado de insaturado.
→ Classificação do carbono na cadeia quanto à geometria
Os carbonos que só realizam ligações simples apresentam geometria tetraédrica. Já os carbonos que realizam uma única ligação covalente dupla, mas duas ligações simples, possuem geometria trigonal plana. Se o carbono, entretanto, apresentar duas ligações duplas ou uma ligação tripla e uma ligação simples, este terá geometria linear.
→ Classificação do carbono na cadeia quanto à hibridização
Na formação da ligação covalente entre átomos, ocorre a combinação linear de orbitais atômicos, originando os orbitais moleculares. Os orbitais moleculares são regiões da molécula em que é provável de se encontrar elétrons.
Átomos de carbono possuem o nível 2 como camada de valência, onde estão os subníveis (ou orbitais) 2s e 2p. Para maior estabilidade, esses orbitais podem se unir, em um efeito conhecido como hibridização. O subnível 2s é formado por um único orbital atômico, enquanto o subnível 2p é formado por três orbitais atômicos. Dessa forma, em uma hibridização, pode haver a combinação do orbital do subnível 2s com até três orbitais do subnível 2p.

Para a formação de um carbono saturado, ou seja, com quatro ligações simples, todos os orbitais atômicos dos subníveis 2s e 2p se combinam, formando o orbital híbrido 2sp3 (ou, simplesmente, sp3). Assim, átomos de carbono que só apresentam ligações simples são classificados quanto à hibridização como sp3.
Quando pensamos em um carbono que faz uma ligação dupla, ele, na verdade, só se liga a três átomos distintos (o qual ele faz a dupla, mais outros dois átomos). Dessa forma, só há necessidade de combinação de três orbitais atômicos: o orbital 2s, mais dois orbitais 2p, gerando o orbital híbrido 2sp2 (ou, simplesmente, sp2). O orbital p que resta, não hibridizado, é utilizado para a formação da ligação adicional, ou seja, a ligação pi. Assim, átomos de carbono que apresentam uma ligação dupla e duas ligações simples são classificados quanto à hibridização como sp2.
Já um átomo de carbono que realiza duas ligações duplas ou uma ligação tripla e uma ligação simples está se ligando, desta forma, a outros dois átomos distintos. Por isso, só há a necessidade de hibridização de dois orbitais atômicos: o orbital 2s e um dos orbitais 2p, gerando o orbital híbrido 2sp (ou, simplesmente, sp). Os orbitais p restantes, os quais não são hibridizados, são utilizados para a formação das ligações adicionais pi. Por isso, todo átomo de carbono que apresenta uma ligação tripla e uma ligação simples, ou duas ligações duplas, é classificado quanto à hibridização como sp.
→ Classificação do carbono na cadeia quanto à simetria (quiralidade)
Átomos de carbono de geometria tetraédrica, quando ligados a quatro grupos distintos, são chamados de assimétricos ou quirais. Assim, carbono quiral é o carbono da cadeia que realiza quatro ligações covalentes com quatro átomos ou grupos atômicos distintos.

Exercícios resolvidos sobre cadeias carbônicas
Questão 1
(Uerj) Observe a fórmula estrutural do fentanil, opioide sintético empregado como anestésico, cujo consumo indiscriminado gera graves consequências:
Na estrutura desse composto, há uma cadeia carbônica fechada presente em maior quantidade.
Essa cadeia é classificada como:
A) alicíclica
B) saturada
C) aromática
D) heterogênea
Resolução:
Alternativa C.
No composto apresentado, há três cadeias carbônicas fechadas. A cadeia mais ao centro é um ciclo alifático (alicíclico) heterogêneo, com o nitrogênio fazendo o papel de heteroátomo. Contudo, os outros dois anéis apresentam todos os carbonos com hibridização sp², além de terem número ímpar de ligações pi. Dessa forma, os dois ciclos restantes (e que estão em maioria) são anéis aromáticos.
Questão 2
(UEMG) Analise a estrutura da molécula e escolha a alternativa que, corretamente, classifique sua cadeia carbônica principal.
CH3–CH2–CH=CH–CH3
A) Cadeia homogênea, insaturada, aberta e ramificada.
B) Cadeia heterogênea, saturada, aberta e linear.
C) Cadeia homogênea, insaturada, aberta e linear.
D) Cadeia heterogênea, insaturada, fechada e ramificada.
Resolução:
Alternativa C.
A cadeia em questão possui carbonos de extremidade e, dessa forma, é classificada como aberta.
É também uma cadeia linear, já que não apresenta ramificações. Também não são observados heteroátomos, o que a coloca como uma cadeia homogênea. Por fim, observa-se uma ligação dupla entre átomos de carbono (...–CH=CH–...), o que é suficiente para classificar a cadeia como insaturada.
Fontes
BRUICE, P. Y. Organic Chemistry. 8. ed. Upper Saddle River, Nova Jersey: Pearson Education Inc., 2015.
MULLER, P. Glossary of terms used in physical organic chemistry (IUPAC Recommendations 1994). Pure and Applied Chemistry, v. 66, n. 5, p. 1086, 1994.
SOLOMONS, T. W. G.; FRYHLE, C. B.; SNYDER, S. A. Química Orgânica: volume 2. 12. ed. Rio de Janeiro: LTC, 2018.