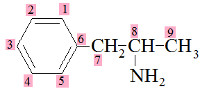
O carbono quiral ou assimétrico é um carbono de hibridização sp3 (geometria tetraédrica) que se liga a quatro grupos totalmente distintos na cadeia carbônica. A presença de carbonos quirais na molécula faz com que sejam sintetizados, na mesma proporção, duas moléculas isômeras, as quais apresentam uma relação de objeto e imagem entre si.
Leia também: Isomeria — o fenômeno que gera compostos distintos com a mesa fórmula molecular
Tópicos deste artigo
- 1 - Resumo sobre o carbono quiral
- 2 - O que é carbono quiral?
- 3 - Exemplos de carbono quiral
- 4 - Características do carbono quiral
- 5 - Como saber se é carbono quiral?
- 6 - Carbono quiral de cadeia fechada
- 7 - Carbono quiral tem ligação dupla?
- 8 - Diferenças entre carbono quiral e aquiral
- 9 - Exercícios resolvidos sobre carbono quiral
Resumo sobre o carbono quiral
- O carbono quiral ou assimétrico é um carbono de hibridização sp3 que se liga a quatro grupos totalmente distintos.
- Carbonos quirais na molécula ocasionam na síntese de isômeros que possuem, entre si, uma relação de objeto e imagem.
- É possível a existência de carbonos quirais tanto em cadeias abertas quanto fechadas.
- Átomos de carbono que realizam ligações duplas ou triplas não podem ser considerados quirais em hipótese alguma.
O que é carbono quiral?

Um carbono é considerado quiral (ou assimétrico) quando ele possui hibridização sp3 (ou seja, de geometria tetraédrica) e se liga a quatro grupos totalmente distintos.
A palavra quiral é de origem grega, significando “mão”. Isso porque moléculas que apresentem carbonos quirais, ao serem sintetizadas, produzem dois isômeros que apresentam, entre si, uma relação de objeto e imagem (ou seja, são não sobreponíveis), tal qual nossas mãos direita e esquerda. Tais isômeros são conhecidos como enantiômeros.
Exemplos de carbono quiral
Diversas são as estruturas orgânicas possíveis de apresentarem carbono quiral. A seguir são apresentados os carbonos quirais (marcados pelo asterisco) presentes em aminoácidos (alanina e fenilalanina) e na molécula do ibuprofeno, medicamento anti-inflamatório amplamente utilizado.

Características do carbono quiral
O carbono quiral, estruturalmente, deve estar ligado a quatro átomos ou grupos completamente diferentes. Para que isso seja possível, ele deve possuir uma geometria tetraédrica (realizar apenas ligações simples) e, consequentemente, uma hibridização do tipo sp3.
A presença de carbonos quirais na molécula permite a geração de enantiômeros, que são isômeros espaciais que apresentam uma relação de objeto e imagem, ou seja, são moléculas de mesma fórmula molecular, mas não são sobreponíveis.
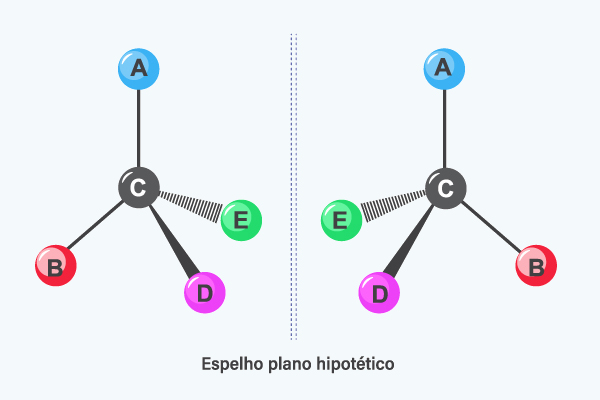
Os enantiômeros apresentam as mesmas propriedades físicas e químicas (em meios reacionais isentos de outras moléculas com carbonos quirais), contudo podem ser distinguidos pela rotação causada num plano de luz polarizada. Assim sendo, se um enantiômero desvia o plano da luz polarizada em 15° para a direita, o outro irá desviar o plano da luz polarizada em 15° para a esquerda.
Leia também: Isomeria óptica — um tipo de isomeria espacial
Como saber se é carbono quiral?
Basicamente, para se identificar um carbono quiral, devemos seguir apenas dois passos, os quais estão dispostos a seguir.
- 1º passo: localize, na molécula, carbonos com hibridização sp3.
- 2º passo: examine os átomos ou grupos atômicos que estão diretamente ligados a esses carbonos. Para que seja quiral, eles devem ser totalmente diferentes.
No exemplo a seguir, o carbono destacado é quiral. Os demais carbonos, apesar de também serem carbonos com hibridização sp3, não são quirais, uma vez que apresentam pelo menos dois átomos de hidrogênio ligados a eles, o que quebra a quiralidade do carbono. Já o carbono destacado está ligado a quatro grupos distintos: um átomo de hidrogênio, um grupo hidroxila, um grupo metil e um grupo etil.

Carbono quiral de cadeia fechada
Devendo apenas apresentar geometria tetraédrica, também é possível que existam carbonos quirais em cadeias fechadas. Contudo, a análise é um pouco distinta. Vejamos os dois exemplos a seguir.
No primeiro exemplo, temos uma cadeia de metilciclopentano.
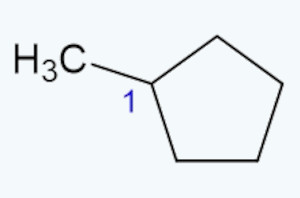
Analisemos se o carbono destacado (o com número 1) é quiral. De fato, apresenta hibridização sp3, mas vejamos se o grupo metil ligado a ele é capaz de torná-lo quiral. Para isso, devemos lembrar que uma cadeia carbônica fechada pode, a partir de um carbono da cadeia, ser analisada em sentido horário ou anti-horário. Se o caminho tomado for o mesmo tanto no sentido horário quanto anti-horário, então o carbono não é quiral.
Isso é o que acontece com o carbono assinalado com número 1 no exemplo anterior. A partir dele, tomando-se o caminho horário, passamos por quatro grupos CH2 (-CH2-CH2-CH2-CH2-) em sequência até chegar ao carbono de número 1 novamente. Tomando-se o caminho anti-horário, a sequência de quatro grupos CH2 se repete até chegar ao carbono de número 1 novamente. Assim sendo, o caminho tomado é o mesmo em ambos os sentidos e, portanto, o carbono de número 1 não é quiral.
Outra maneira de se observar a quiralidade ou não de um carbono em uma cadeia fechada é por meio de um método em que se traça uma linha que passe pelo suposto carbono quiral e o centro da cadeia fechada ao mesmo tempo, como demonstrado a seguir.

Repare que a linha tracejada divide o anel de cinco carbonos em duas metades idênticas. Como essas metades são idênticas, então o carbono assinalado com o número 1 não é quiral.
Agora analisemos um segundo exemplo, que se trata do composto 2-metilciclopentan-1-ol. O carbono a ser avaliado como quiral foi, novamente, marcado com o número 1.

Repare que ao se tomar, a partir do carbono assinalado com o número 1, o caminho horário, teremos o seguinte: -CHOH-CH2-CH2-CH2-. Já quando tomamos o caminho anti-horário, o caminho descrito a partir do carbono assinalado com o número 1 é -CH2-CH2-CH2-CHOH-. Assim, é possível perceber que os caminhos são diferentes e, dessa forma, concluímos que o carbono assinalado com o número 1 é quiral.
Pelo outro método, a partir da linha que passa pelo suposto carbono quiral e o centro da cadeia fechada, também conseguimos observar a quiralidade desse carbono, já que as metades obtidas são distintas (uma possui o grupo hidroxila, enquanto a outra metade não).

Com base no que foi descrito, também é possível perceber que o carbono ligado ao grupo hidroxila também é quiral.
Carbono quiral tem ligação dupla?
O carbono quiral não pode apresentar ligação dupla. Como foi dito anteriormente, é necessário que ele tenha hibridização sp3 e esteja ligado a quatro grupos completamente diferentes. Os carbonos com ligação dupla apresentam hibridização sp2, uma geometria plana.
Ao adotarem essa geometria, não é possível que as moléculas formadas sejam enantiômeros, ou seja, compostos que apresentam relação de objeto e imagem (não são sobreponíveis).
Diferenças entre carbono quiral e aquiral
Os carbonos aquirais são aqueles que não contemplam as condições para serem quirais. Vale lembrar que para ser um carbono quiral, o carbono deve:
- apresentar hibridização sp3 e;
- estar ligado a quatro grupos distintos.
Assim sendo, caso um dos critérios não seja obedecido, o carbono será considerado como aquiral. No exemplo a seguir é possível perceber melhor essa distinção.

Repare que apenas o carbono assinalado com o número 3 é quiral, pois atende aos dois critérios necessários para ser quiral. Os carbonos assinalados com os números 1 e 2 não podem ser quirais, uma vez que apresentam hibridização sp2 (uma ligação dupla). Já os carbonos assinalados com os números 4, 5 e 6 são aquirais, pois apresentam ligações com grupos iguais. No caso do carbono com o número 4, ele se liga a dois grupos metil, enquanto os outros dois (5 e 6), ligam-se com três átomos de hidrogênio.
Leia também: Quais são os tipos de isomeria?
Exercícios resolvidos sobre carbono quiral
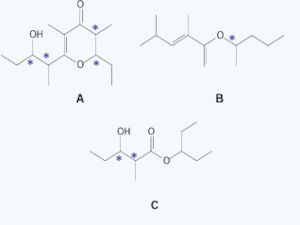
Questão 1. (UFG – Vespertino/2025.2) Os feromônios são substâncias que promovem a comunicação química entre os insetos. Existem diversos tipos, como os feromônios sexuais, de agregação, de alarme, entre outros. Nessa comunicação, a estrutura química e o arranjo espacial dos átomos têm papel fundamental. Três exemplos de feromônios de insetos são representados a seguir.

Nas estruturas dos feromônios A, B e C, o número de estereocentros (carbonos quirais) respectivamente é:
- 5, 2 e 1.
- 4, 1 e 3.
- 4, 1 e 2.
- 5, 2 e 2
- 3, 2 e 3.
Resposta: Letra C.
A imagem a seguir aponta, com um asterisco, os carbonos quirais dos feromônios A, B e C.
Questão 2. (Unesc 2025.1) Na química orgânica, a configuração espacial dos átomos em uma molécula pode influenciar suas propriedades e reações. Um aspecto importante nesse contexto é o carbono quiral, que desempenha um papel crucial na formação de isômeros ópticos.
Observe a estrutura química do composto orgânico abaixo.

Quantos carbonos quirais esse composto orgânico apresenta?
- 1
- 2
- 3
- 4
- 5
Resposta: Letra B.
Os carbonos quirais do composto orgânico estão marcados por um asterisco na imagem a seguir.

Fontes:
SOLOMONS, T. W. G.; FRYHLE, C. B.; SNYDER, S. A. Química Orgânica: volumes 1 e 2. 12. ed. Rio de Janeiro: LTC, 2018.
BRUICE, P. Y. Organic Chemistry. 8. ed. Upper Saddle River, Nova Jersey: Pearson Education Inc., 2015.
INTERNATIONAL UNION OF PURE AND APPLIED CHEMISTRY – IUPAC. GoldBook – Compendium of Chemical Terminology. Disponível em: < https://goldbook.iupac.org/>. Acesso em 13 jul. 2024.